Химия. 10 класс
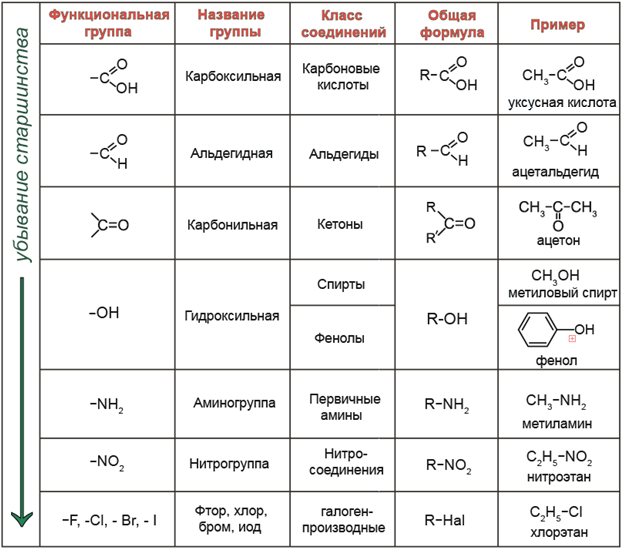
Удобная навигация, видео-разборы тем, задачи для самопроверки — всё это в вашем кармане. А ещё раздел с полезными материалами, календарь занятий и уведомления о предстоящих уроках. Понятие г ибридизации электронных орбиталей.



/Zakharova.files/image011.jpg)
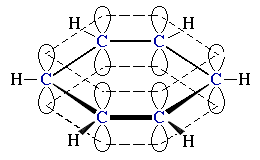

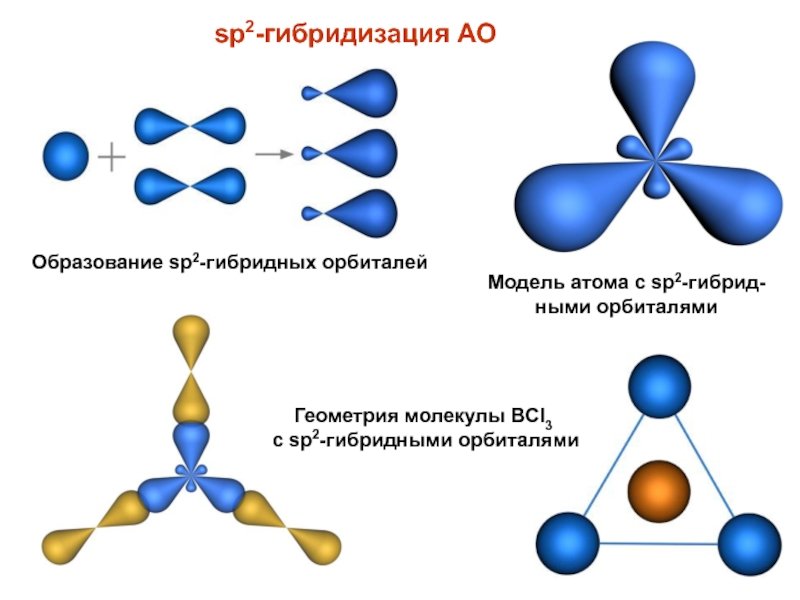
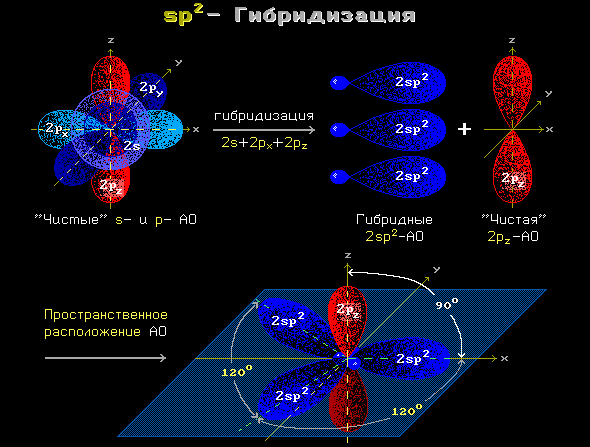
Часто химические связи образуются за счёт электронов, расположенных на разных атомных орбиталях. Казалось бы, и связи в молекуле по прочности должны быть неравноценными. Однако опыт показывает, что они равнозначны.
- Атом состоит из положительно заряженного ядра и находящихся в его поле отрицательно заряженных электронов. Число электронов в атоме химического элемента равно положительному заряду ядра атома и порядковому номеру элемента в ПСХЭ.
- Ковалентная химическая связь образуется при помощи общих связывающих электронных пар по типу:. Образовывать химическую связь, то есть создавать общую электронную пару с «чужим» электроном от другого атома, могут только неспаренные электроны.
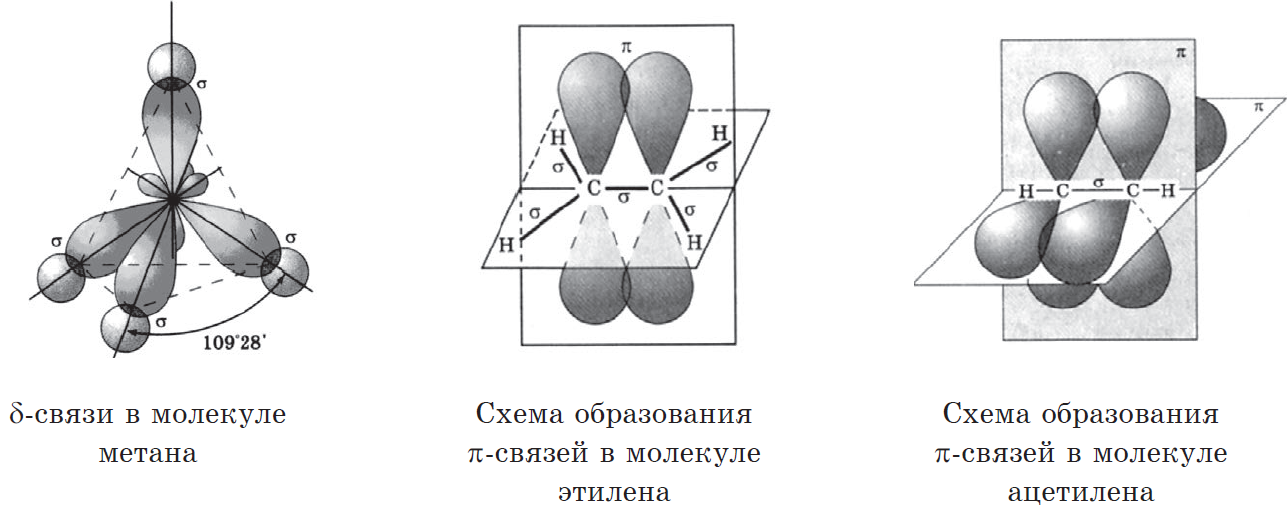
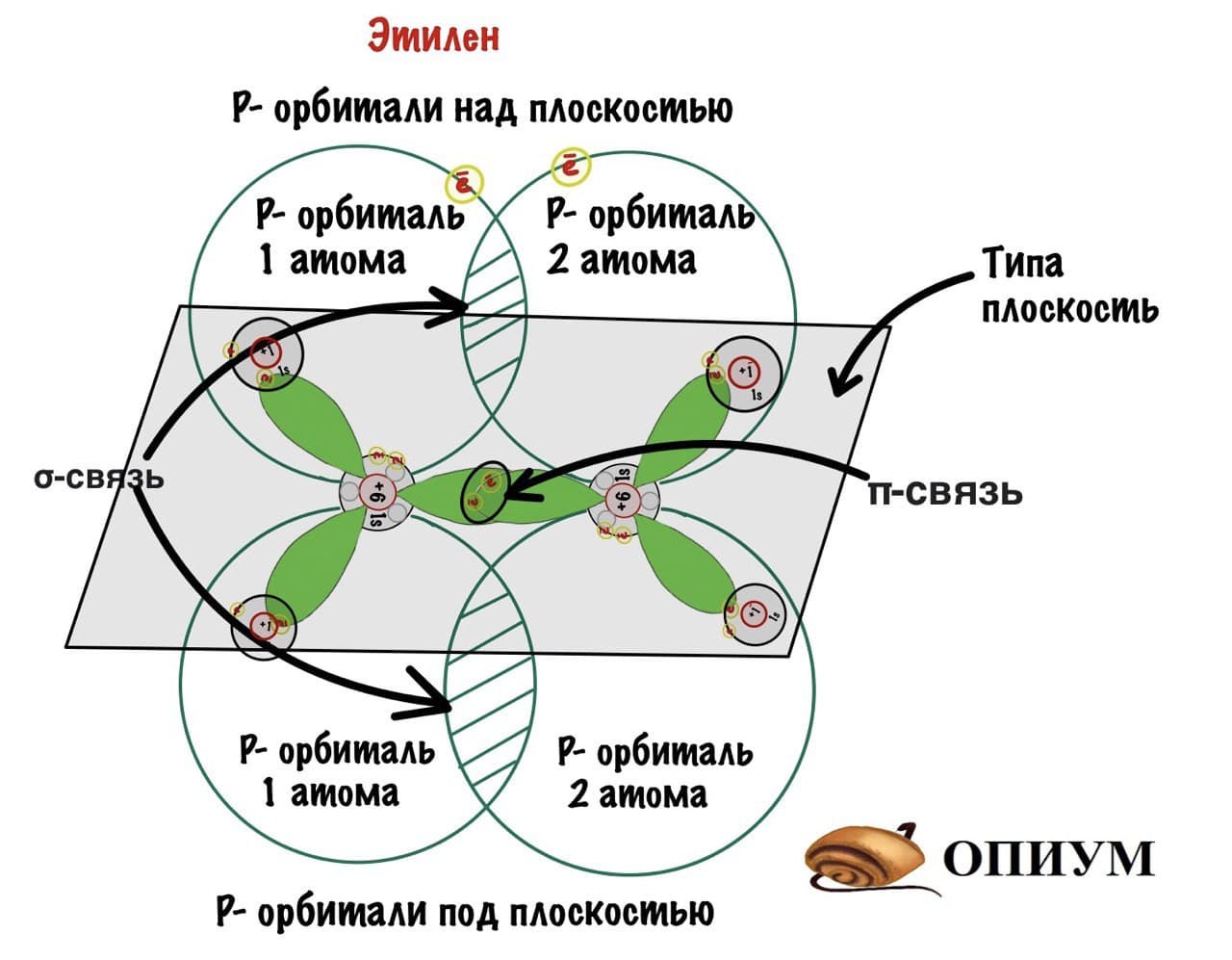
- Изучая строение молекул органических веществ, вы узнали, что все молекулы имеют определённое пространственное строение.
- Изучить литературу по теме исследования.
- Актуальность работы. К настоящему времени установлено, что алмаз является тревосходвым материалом для создания электронных приборов.
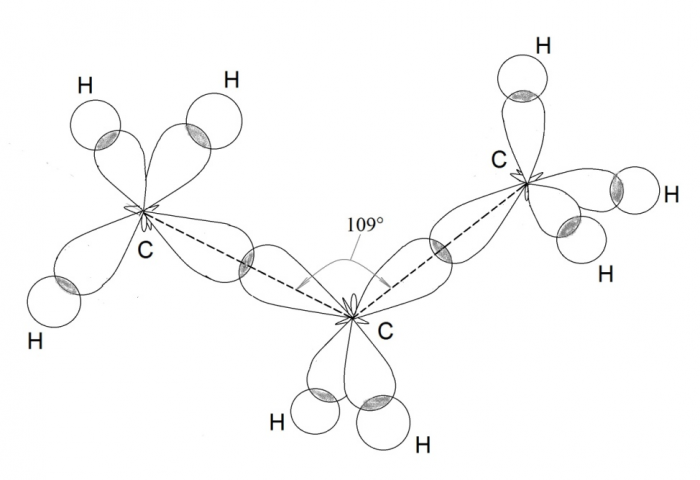
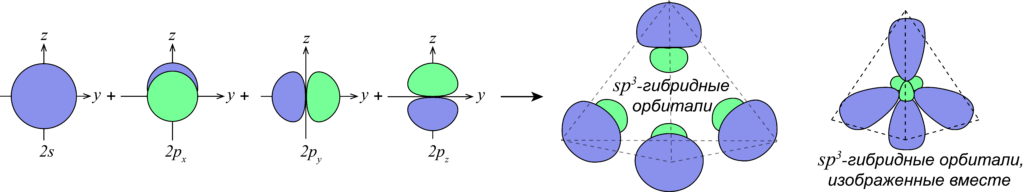
- Все изображения из подборки Идеи для срисовки гибридизация sp3 можно скачать и просмотреть бесплатно. Также вы можете поделиться содержимым с друзьями в социальных сетях и мессенджерах.
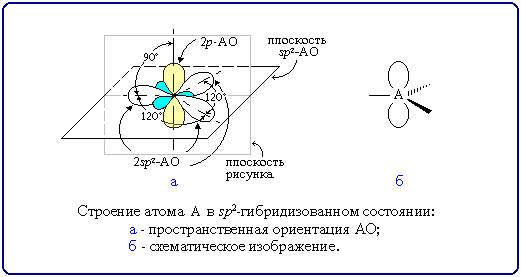



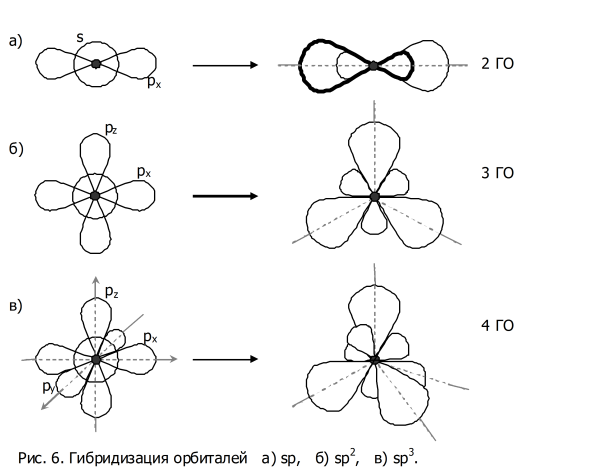


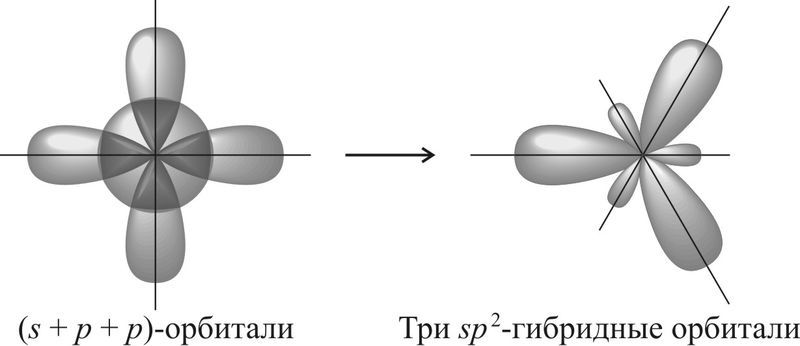

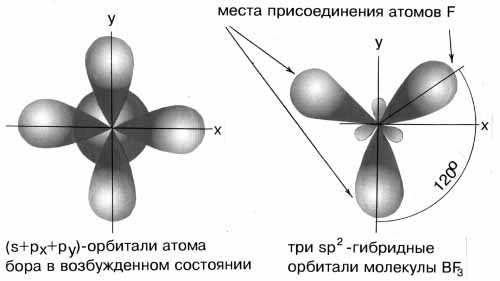

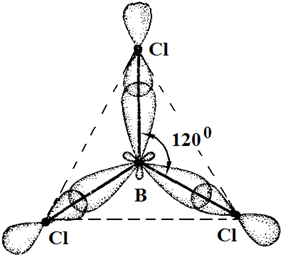
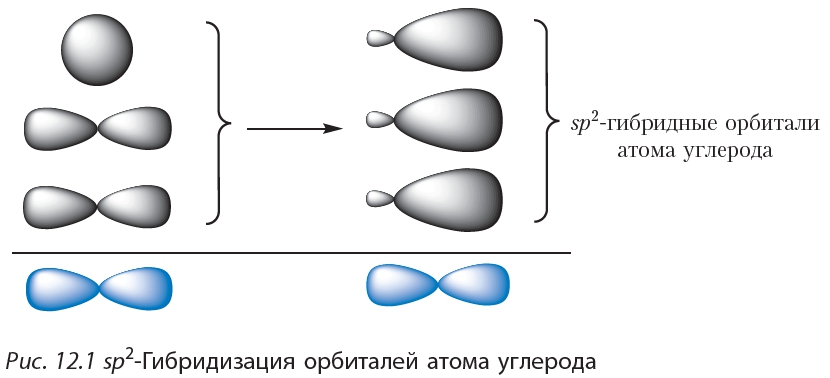
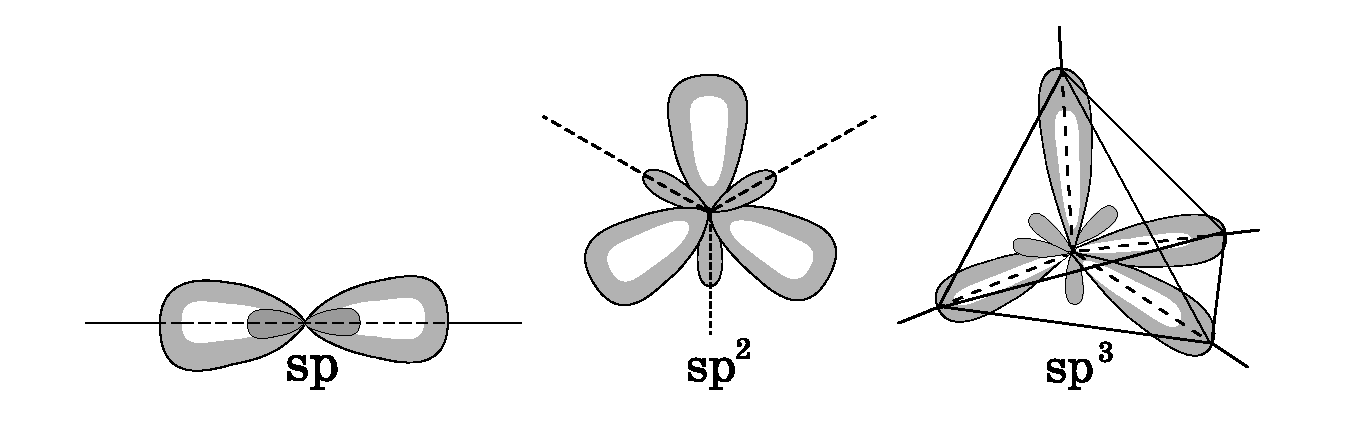
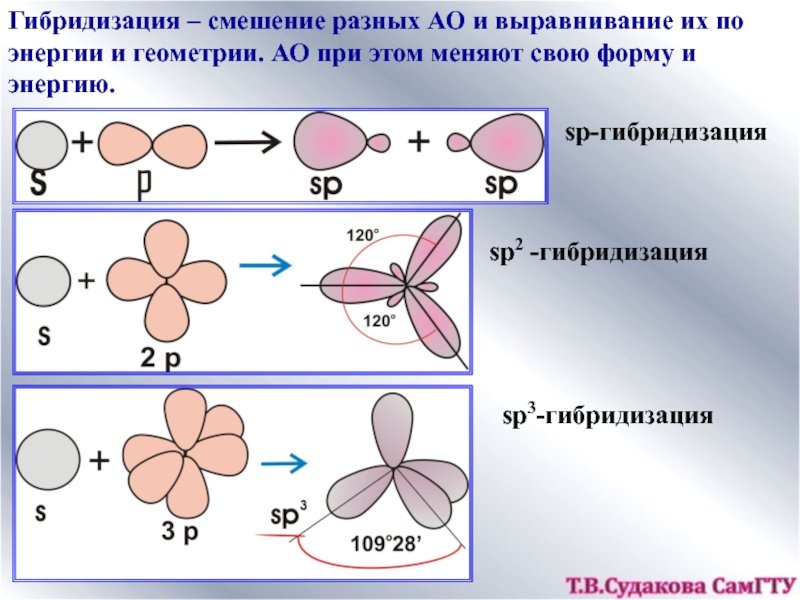
В образовании ковалентных связей принимают участие электроны, орбитали которых могут иметь разную форму и разную ориентацию в пространстве. Но во многих соединениях химические связи оказываются равноценными. Для объяснения этого явления Полинг предложил ввести понятие «гибридизация».